第一类医疗器械备案是医疗器械市场准入的重要步骤。为了帮助企业顺利通过备案过程,以下是五个关键要点,需要企业在备案前充分理解和准备。
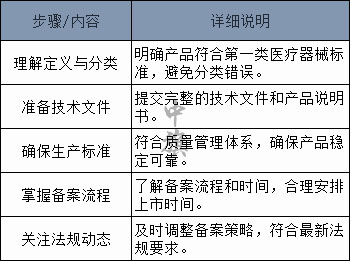
第一类医疗器械指的是在正常使用条件下,对人体的安全性和有效性风险较低的设备。企业在申报前,需确保其产品符合第一类医疗器械的分类标准,避免分类错误导致备案失败。
备案过程中,必须提交完整的技术文件和产品说明书。这些文档应详细描述产品的设计、制造过程、功能、使用方法以及安全性评估,确保监管机构能够全面了解产品特性。
第一类医疗器械的生产企业需要符合特定的质量管理体系。生产环境、设备、人员培训及产品质量控制措施必须达到国家规定的标准,以保证产品的稳定性和可靠性。
了解具体的备案流程和所需时间对于规划产品上市至关重要。备案流程通常包括提交备案文件、等待审查、补充材料等阶段。企业应提前准备并合理安排时间,避免影响产品上市计划。
医疗器械行业的法规经常更新,企业应持续关注相关法规、标准的变化以及行业动态。及时调整备案策略和产品设计,以符合最新的法规要求,保障备案的顺利进行。
本文链接: https://www.zqsws.com/mfwz/219.html 未经授权,禁止转载。
下一篇:你的网站办理了EDI许可证吗?